靶向脂質體載藥藥物
脂質體共價連接藥物-脂質偶聯載***式通過連接劑將藥物分?與脂質共價連接是另?種在脂質體內裝載藥物的有效策略,例如Mepact。MDP是主要?蘭?陽性菌細胞壁的組成部分,具有****應答的作?。由于MDP是?溶性低分?量分?,其脂質體在儲存過程中存在包封效率低和藥物泄漏等問題。為了提?MDP的脂溶性,通過肽間隔劑將MDP與PE連接,合成MTP-PE(muramyltripeptide-phosphatidylethanolamine)。在??理鹽?重建凍?產物(MTP-PE,POPC和OOPS)時,MTP-PE的兩親分?嵌?脂質體的膜雙層。脂質體內存在MTP-PE,未發現游離MTP-PE。Vyxeos采?被動加載和主動加載相結合的?法,這是?個被批準在同?囊泡中加載兩種不同藥物(阿糖胞苷和柔紅霉素)的脂質體。簡??之,當脂質泡沫與Cu(葡糖酸鹽)2、三?醇胺(TEA)、pH7.4和阿糖胞苷溶液?合時,阿糖胞苷被被動地封裝到脂質體中。經過減漿和緩沖液交換以去除未包封的藥物和Cu(葡糖酸鹽)2/TEA后,中性pH的柔紅霉素緩沖液與載糖胞苷脂質體孵育。不同類型的脂質體在體內代謝過程中在代謝穩定性、代謝產物、對藥物代謝的影響變化等方面存在差異。靶向脂質體載藥藥物
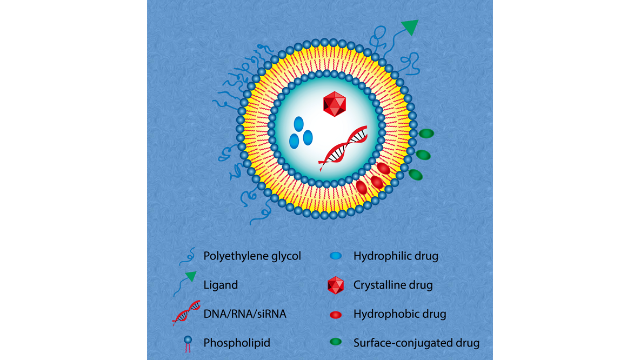
為了***免疫性疾病,將針對甘油醛3-磷酸脫氫酶(***DH)的siRNA與含1,2-dilinoleyl-4-(2-dimethylaminoethyl)-[1,3]-dioxolane、DSPC和膽固醇的陽離子脂質體絡合。用該復合物(5mg/kgsiRNA)處理小鼠,4天后,腹腔巨噬細胞和樹突狀細胞的***DH表達量減少40%,脾源性抗原呈遞細胞的***DH表達量減少60%。在其他研究中,將重鏈鐵蛋白特異性siRNA與陽離子脂質體結合,并局部給藥于荷U251細胞的人膠質瘤小鼠。**內注射鐵蛋白特異性siRNA與DC-Chol和DOPE組成的陽離子脂質體復合物,其抑制**生長的程度與卡莫司定(一種主要用于膠質瘤***的DNA烷基化劑)相當。argonaute-2特異性siRNA已被證明可誘導細胞凋亡,使用由DC-6-14、DSPC、DOPE和DSPC-PEG2000組成陽離子脂質體遞送argonaute-2特異性siRNA時發現,將這些復合物靜脈注射到接種Lewis肺*的小鼠體內(每隔一天1mg/kg,共5次),這些復合物可降低**組織中argonaute-2的表達,并***抑制**生長。青海蘇州脂質體載藥由于耐藥細菌的出現和傳播,改進現有的藥物傳遞系統至關重要。

PEG的低分?量(<750Da)顯?出不***的空間穩定作?[58]。此外,當PEG-DSPE在脂質組合中的濃度為7±2mol%時,脂質體的?物穩定性**?,?在體內使?的peg-脂質偶聯物的典型濃度為5mol%(例如Doxil)。當PEG-DSPE濃度低于4mol%時,PEG鏈呈“蘑菇”狀,厚度約為3.5nm。隨著濃度增加4-8mol%,PEG鏈的構型轉變為“刷狀”,厚度為4.5-10nm。進?步增加摩爾?,形成膠束?不是脂質體組裝。綜上所述,PEG2000在脂質體中的作用包括增強穩定性、延長血液循環時間、降低免疫原性以及調控藥物釋放,使其成為藥物輸送系統設計中常用的功能性修飾劑。
脂質體靶向遞送中葉酸配體修飾脂質與生物活性小分子(如葉酸)的結合已被研究用于靶向遞送核酸。例如,由葉酸與1-棕櫚酰-2-油酰-sn-甘油-3-非共價結合而形成的脂質體乙基磷脂膽堿:膽固醇脂質體顯著提高胸苷激酶質粒DNA轉染效率,抑制體外TSA和SCC7細胞生長。這些葉酸相關的脂質體在移植SCC7**的小鼠中顯示出較高的抗**效果。在另一種方法中,葉酸標記的陽離子脂質體與小牛胸腺DNA復合物***巨噬細胞,與不含葉酸的普通陽離子脂質體相比,顯示出更高的DNA葉酸受體表達細胞的遞送。在荷瘤小鼠中,與不含葉酸的脂質體相比,葉酸標記的脂質體誘導干擾素-g和白細胞介素-6的產生,延長了存活時間。甘草次酸已被用于靶向肝細胞肝*細胞,基于一項研究表明,與鄰近的非**肝細胞相比,甘草次酸的結合靶點蛋白激酶C在肝細胞*細胞表面的表達更高。合成了甘次酸-次酸-聚乙二醇-聚膽甾醇綴合物,并將其與DOTAP和膽固醇配制成陽離子脂質體。這些脂質體與表達GFP的質粒DNA形成復合物的能力更高,并且與缺乏甘次酸的對照陽離子Lipo脂質體相比,能增強質粒DNA轉染至肝*細胞的能力。表面活性劑對脂質體藥物體內穩定性具有多方面的影響。
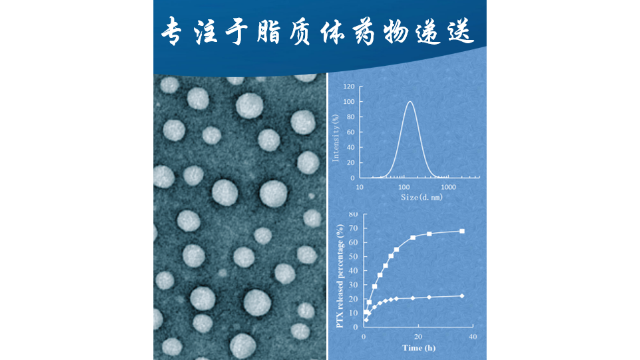
修飾脂質體實現靶向給藥利用超重力設備技術實現脂質體連續化生產,以索拉非尼為模型藥優化制備條件。加入抗氧化劑白藜蘆醇可提高脂質體的穩定性,在體外抗**實驗中增強了索拉非尼對HepG-2細胞的抑制作用。合成尤特奇-凝集素并包覆在脂質體表面,使其能夠用于靶向給藥,提高藥物的生物利用度16。靶向給藥可以將藥物準確輸送到病變部位,減少藥物在非目標部位的分布,降低副作用,提高生物利用度。六、改進脂質體制劑提高藥物的生物利用度和抗***活性制備聚乙烯乙二醇琥珀酸維生素E修飾的載有漆黃素(PCB)的脂質體(PCBT-脂質體)。PCBT-脂質體顯示出球形和雙層納米顆粒,具有高藥物包封效率和良好的儲存穩定性。在四種不同pH介質中的累積釋放率明顯高于游離PCB。體內研究表明,PCBT-脂質體可明顯提高PCB的口服生物利用度,同時降低糖尿病小鼠血清中的生化指標濃度17。這種新型脂質體制劑通過提高藥物的溶解度和穩定性,改善了藥物的生物利用度和抗***活性。不對稱脂質體是一種具有獨特結構的脂質體,其內外層由不同的脂質組成。山東microbubble脂質體載藥
脂質體作為一種極具潛力的藥物載體,在藥物遞送領域發揮著重要作用。靶向脂質體載藥藥物
基于維生素CpH/離子梯度的主動藥物載入新方法。通過調節外部pH值、載入時間和藥物與脂質的比例等參數,實現***藥物表柔比星(EPI)的載入。EPI與維生素C共同封裝可以增加其***活性,可能是通過協同作用實現的。此外,由于EPI維生素C鹽的良好溶解性,這種方法可以使藥物更快地從脂質體中釋放,從而增加脂質體制劑的***活性5。綜上所述,脂質體載藥的原理主要包括利用脂質體的結構特點,通過不同的載藥技術將親水***物和親脂***物載入脂質體中,以及采用酶敏感載藥和維生素CpH/離子梯度載藥等特殊方法,以提高藥物的包封率和穩定性,增強藥物的***效果并降低藥物毒性。靶向脂質體載藥藥物
- 靶向脂質體載藥藥物 2025-02-15
- 全氟烷脂質體載藥動物實驗 2025-02-15
- 遼寧肺靶向脂質體載藥 2025-02-15
- 河北成都脂質體載藥 2025-02-15
- 提供脂質體載藥成像 2025-02-15
- 青海蘇州脂質體載藥 2025-02-15
- 濟南脂質體載藥包裹藥物 2025-02-15
- 內蒙古陽離子轉染試劑 2025-02-15
- 浙江微流控脂質體載藥 2025-02-15
- 青海免疫熒光熒光染料 2025-02-15
- 銀杏肽口服液工廠 2025-02-15
- 湖北一次性使用病毒采樣管廠家 2025-02-15
- 哈森型穿刺器品牌 2025-02-15
- 天津養生艾灸加盟條件 2025-02-15
- 上海國產水門汀公司 2025-02-15
- 南京胸部按摩緊致套售價 2025-02-15
- 江蘇3M環氧乙烷滅菌價格 2025-02-15
- 安徽口服膠囊yFMT美益添 2025-02-15
- 上海康養中心艾灸儀 2025-02-15
- 浙江帶電尼龍膜定做 2025-02-15