天津正規(guī)外泌體提取試劑單價(jià)
外泌體,是一種能被大多數(shù)細(xì)胞分泌的微小膜泡,具有脂質(zhì)雙層膜結(jié)構(gòu),直徑大約40-100nm。盡管外泌體較初在1983年就被發(fā)現(xiàn),但人們一直認(rèn)為它只是一種細(xì)胞的廢棄物。然而較近幾年,人們發(fā)現(xiàn)這種微小膜泡中含有細(xì)胞特異的蛋白、脂質(zhì)和核酸,能作為信號(hào)分子傳遞給其他細(xì)胞從而改變其他細(xì)胞的功能。這些發(fā)現(xiàn)點(diǎn)燃了人們對(duì)細(xì)胞分泌膜泡的興趣。較近的研究發(fā)現(xiàn)外泌體在很多生理病理上起著重要的作用,如免疫中抗原呈遞、一些病癥的生長(zhǎng)與遷移、組織損傷的修復(fù)等。不同細(xì)胞分泌的外泌體具有不用的組成成分和功能,可作為疾病診斷的生物標(biāo)志物。多種細(xì)胞在正常及病理狀態(tài)下均可分泌外泌體。天津正規(guī)外泌體提取試劑單價(jià)

外泌體的提取、分離方法:梯度密度離心法。研究發(fā)現(xiàn),外泌體的密度在1.1~1.19kg·L-1之間,因此,可以采用密度梯度離心法來(lái)分離外泌體。該方法是將超速離心結(jié)合蔗糖密度梯度或蔗糖墊結(jié)合,原理是先除去非囊泡物質(zhì),再通過(guò)梯度密度濃縮提取外泌體,該方法可以得到相對(duì)較為純凈的外泌體。傳統(tǒng)的梯度密度方法通常需要離心16h,但是2012年,研究者[15]使用了62~90h才分離出某些確切囊泡,因此,該方法可能不足以沉淀所有的外泌體。如果離心時(shí)間不充足,污染物質(zhì)可能和外泌體保持在相同的密度層,特別是這個(gè)密度范圍又比較寬。鄭州外泌體提取試劑生產(chǎn)廠家目前人們多采用超速離心、免疫磁珠、超濾、沉淀或試劑盒等方法實(shí)現(xiàn)外泌體的提取分離。
PS不是你想有,想有就能有,迄今為止所發(fā)現(xiàn)的外泌體,并非所有的外膜表面都暴露PS。例如,細(xì)菌來(lái)源的外泌體膜表面沒(méi)有PS,因此,本款試劑不能提取這種外泌體。現(xiàn)在的研究尚未得知是否所有的外泌體上都會(huì)露出PS,但是上述的外泌體標(biāo)記根據(jù)細(xì)胞種類不同表現(xiàn)出的信號(hào)強(qiáng)弱差大,通過(guò)利用本試劑盒PS親和法捕捉、提取外泌體是較好的方法。:這個(gè)MagCapture?ExosomeIsolationKitPS,1次提取的外泌體量大概是多少?實(shí)驗(yàn)樣品的種類和體積不同,提取的外泌體量也不一樣。Wako的操作實(shí)例中,一次提取操作可獲得蛋白量約30μg/mL(BCA法檢測(cè)),粒子數(shù)1~2×1010(NanoSightLM10檢測(cè))(經(jīng)莫能菌素鈉刺激外泌體分泌的K562培養(yǎng)上清5mL濃縮為1mL后,對(duì)其進(jìn)行提取)。另外,和光驗(yàn)證了從1mL正常人混合血清提取一次,可回收約34μg/mL蛋白質(zhì)(BCA法檢測(cè)),約5×109/mL的粒子數(shù)(NanoSightLM10檢測(cè))。本試劑盒終可獲得100μL的洗脫液。
外泌體的提取分離:1、PEG-base沉淀法。聚乙二醇(PEG)可與疏水性蛋白和脂質(zhì)分子結(jié)合共沉淀,早先應(yīng)用于從血清等樣本中收集病毒,現(xiàn)在也被用來(lái)沉淀外泌體,其原理可能與競(jìng)爭(zhēng)性結(jié)合游離水分子有關(guān)。利用PEG沉淀外泌體存在不少問(wèn)題:比如純度和回收率低,雜蛋白較多(假陽(yáng)性),顆粒大小不均一,產(chǎn)生難以去除的聚合物,機(jī)械力或者吐溫-20等化學(xué)添加物將會(huì)破壞外泌體等,因此發(fā)表文章時(shí)易受質(zhì)疑。2、試劑盒提取。近幾年來(lái),市場(chǎng)上已出現(xiàn)各種商業(yè)化的外泌體提取試劑盒,有的是通過(guò)特殊設(shè)計(jì)的過(guò)濾器過(guò)濾掉雜質(zhì)成分,有的則采用空間排阻色譜法(SEC)進(jìn)行分離純化,也有的則利用化合物沉淀將法外泌體沉淀出來(lái)。這些試劑盒不需要特殊設(shè)備,隨著產(chǎn)品不斷更新?lián)Q代,提取效率和純化效果逐漸提高,因而逐漸取代超速離心法并推廣開(kāi)來(lái)。有些試劑盒操作簡(jiǎn)便,不用超速離心,同時(shí)可獲得高純度和高回收率的外泌體。外泌體的提取、分離方法:開(kāi)發(fā)高效、快速、穩(wěn)定,并且保持外泌體結(jié)構(gòu)和生物功能完整性的方法。

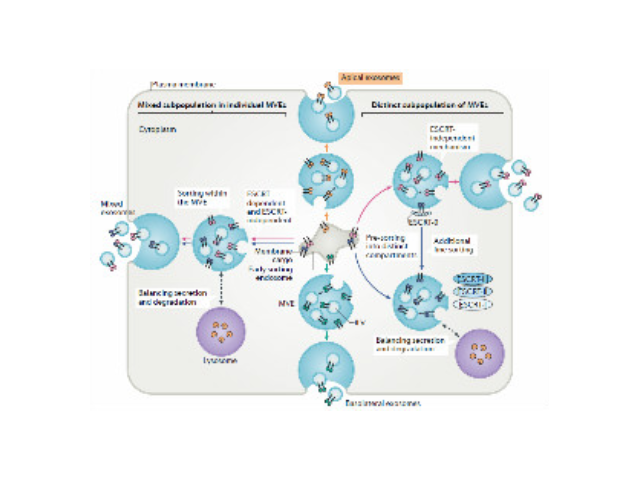
1983年,外泌體初次于綿羊網(wǎng)織紅細(xì)胞中被發(fā)現(xiàn),1987年Johnstone將其命名為“exosome”。多種細(xì)胞在正常及病理狀態(tài)下均可分泌外泌體。其主要來(lái)源于細(xì)胞內(nèi)溶酶體微粒內(nèi)陷形成的多囊泡體,經(jīng)多囊泡體外膜與細(xì)胞膜融合后釋放到胞外基質(zhì)中。所有培養(yǎng)的細(xì)胞類型均可分泌外泌體,且外泌體天然存在于體液中,包括血液、唾液、尿液、腦脊液和乳汁中。有關(guān)他們分泌和攝取及其組成、“運(yùn)載物”和相應(yīng)功能的精確分子機(jī)制剛剛開(kāi)始研究。外泌體目前被視為特異性分泌的膜泡,參與細(xì)胞間通訊,對(duì)外泌體的研究興趣日益增長(zhǎng),無(wú)論是研究其功能還是了解如何將其用于微創(chuàng)診斷的開(kāi)發(fā)。如何高效地提取外泌體是實(shí)現(xiàn)這項(xiàng)新興液體活檢技術(shù)臨床常規(guī)化應(yīng)用的關(guān)鍵。外泌體:形成了一種全新的細(xì)胞間信息傳遞系統(tǒng),影響細(xì)胞的生理狀態(tài)并與多種疾病的發(fā)生與進(jìn)程密切相關(guān)。石家莊正規(guī)外泌體提取試劑生產(chǎn)廠家
外泌體目前被視為特異性分泌的膜泡,參與細(xì)胞間通訊。天津正規(guī)外泌體提取試劑單價(jià)
外泌體的提取分離:1、超速離心法(差速離心)。超離法是常用的外泌體純化手段,采用低速離心、高速離心交替進(jìn)行(如圖所示),可分離到大小相近的囊泡顆粒。超離法因操作簡(jiǎn)單,獲得的囊泡數(shù)量較多而廣受歡迎,但過(guò)程比較費(fèi)時(shí),且回收率不穩(wěn)定(可能與轉(zhuǎn)子類型有關(guān)),純度也受到質(zhì)疑;此外,重復(fù)離心操作還有可能對(duì)囊泡造成損害,從而降低其質(zhì)量。2、密度梯度離心。在超速離心力作用下,使蔗糖溶液形成從低到高連續(xù)分布的密度階層,是一種區(qū)帶分離法。通過(guò)密度梯度離心,樣品中的外泌體將在1.13-1.19g/ml的密度范圍富集。此法獲得的外泌體純度較高,但步驟繁瑣,耗時(shí)。天津正規(guī)外泌體提取試劑單價(jià)
- 合肥無(wú)血清細(xì)胞凍存液廠家推薦 2025-04-24
- 南昌正規(guī)外泌體提取試劑直銷價(jià) 2025-04-24
- 上海武漢鼠尾膠原 2025-04-24
- 金華正規(guī)外泌體提取試劑價(jià)格 2025-04-24
- 唐山RNA提取試劑進(jìn)貨價(jià) 2025-04-24
- 徐州開(kāi)封無(wú)血清細(xì)胞凍存液 2025-04-24
- 南昌無(wú)血清細(xì)胞凍存液推薦廠家 2025-04-24
- 廈門無(wú)血清細(xì)胞凍存液哪里買 2025-04-24
- 重慶正規(guī)RNA提取試劑單價(jià) 2025-04-24
- 武漢鼠尾膠原廠家直銷 2025-04-24
- 新疆水基防銹劑誠(chéng)信合作 2025-04-24
- 南昌正規(guī)外泌體提取試劑直銷價(jià) 2025-04-24
- 廣東棕色干燥器現(xiàn)貨 2025-04-24
- 浙江本地防腐涂料銷售廠家 2025-04-24
- 加美國(guó)六機(jī)油值得買嗎 2025-04-24
- 上海防銹紙服務(wù)至上 2025-04-24
- 陜西環(huán)保水基防銹劑價(jià)格 2025-04-24
- 天津水溶性水性清洗劑生產(chǎn) 2025-04-24
- 山東PS磷脂酰絲氨酸食品廠商 2025-04-24
- 長(zhǎng)效環(huán)保機(jī)油哪里產(chǎn)的 2025-04-24