西藏高質量臨床前動物實驗研究
臨床前動物實驗除了《藥物非臨床研究質量管理規范》第十五至十七條對研究設備的基本要求之外,鑒于醫療器械動物實驗研究通常非常復雜,其所用特殊設備可能會從委托方向合同研究機構轉移,因此,建議委托方與顧問和專題負責人仔細研究實驗中使用的合同設備保養、維護的相關知識。參與臨床前動物實驗研究計劃的人員應與將實際實施研究的人員盡早進行頻繁的交流,以確保研究設施擁有用于研究的適當輔助設備和資源。特殊設備的轉移流程及認證、培訓、使用應制定相應的SOP,做好設備使用記錄。化學藥臨床前動物實驗外包;西藏高質量臨床前動物實驗研究

醫療器械臨床試驗前動物試驗研究,作為在臨床試驗之前初步驗證醫療器械安全性及有效性的手段,對于尚沒有大量臨床應用歷史的高風險醫療器械以及創新型醫療器械來說是必要的試驗。我國在2016年3月23日發布了《醫療器械臨床試驗質量管理規范》,在該管理規范中,明確要求在臨床試驗研究之前申請者應當完成必要的動物試驗研究以及風險分析。關于是否需要做臨床前動物試驗研究應根據產品的風險分析進行判斷。2019年4月19日,國家藥品監督管理局(NMPA)發布了《醫療器械動物實驗研究技術審查指導原則***部分:決策原則》,對如何決策是否有必要進行臨床前動物實驗研究給出了指導性建議。重慶靠譜臨床前動物實驗生物藥臨床前動物實驗指導原則;
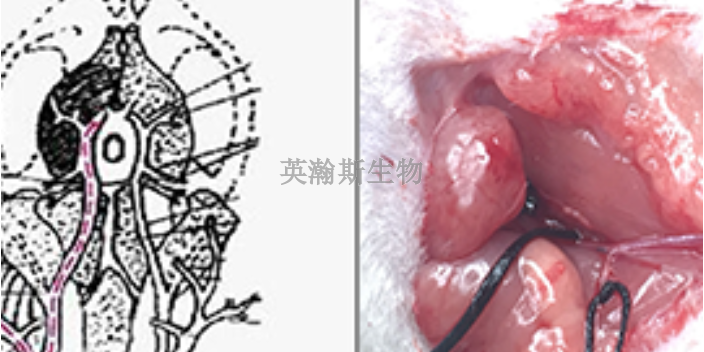
臨床前動物實驗,TGN1412是TeGenero的較早產品,從生產到進入臨床試驗才2年多時間,從MHRA批準TGN1412進入臨床試驗到試驗開始總共才45天。ESG指出,雖然臨床前動物實驗沒有發現嚴重不良反應,但不能因此估測出一個TGN1412用于人類的安全劑量,藥物的安全性未得到充分論證。實施臨床試驗的研究者沒有受到良好培訓,志愿者對可能發生的危險也了解不足。媒體和公眾都指責MHRA為了吸引醫藥公司到英國進行臨床研究而放寬了藥物臨床研究的審批。從而使一家*有15名雇員、風險資本驅動的德國小公司不在本國進行臨床試驗,卻轉而選擇英國。
臨床前動物實驗的計劃和實驗方案制定:首先,臨床前動物實驗研究必須經過周密計劃。為此,實驗計劃需要有一定資質的機構或者個人提出,由有適當資質和經驗的指定的專題負責人進行指導。專題負責人宜在實驗場所辦公,便于指導和監督實驗技術的實施。專題負責人負責研究結果的解釋、分析、形成文件和報告。實驗方案應包括《藥物非臨床研究質量管理規范》第八章第二十九條中所要求的適用于一般GLP方案的十五項要素,并宜包含如特殊環境下的研究規范(操作指南)。任何**終已通過的實驗方案的改變和修改以及修改原因都必須經由專題負責人簽字并簽署日期。實驗方案和任何修改必須提供給質量保證部門檢查。研究開始前需要先通過動物倫理委員會對已確定的實驗方案進行審批。化學藥臨床前動物實驗中心;

申請人應盡臨床前動物實驗的可能通過初步研究(如實驗室研究等)來驗證所確定的風險控制措施的有效性,只有在實驗室研究不足時,才能通過動物實驗進行進一步驗證。動物實驗數據可作為風險/收益分析的支持數據。1.可行性研究:可行性研究是指在產品設計和開發階段,為確認/驗證產品的工作原理、作用機理、設計、可操作性、功能性、安全性等方面,或識別新的意外風險而進行的研究。2.安全性研究:申請人采取風險控制措施后,可通過動物實驗對部分產品的安全性進行適當評價。3.有效性研究:盡管某些醫療器械在動物和人類之間的有效性可能存在一些差異,但合理設計的動物實驗可以支持產品的有效性(包括性能和操作)。化妝品臨床前動物實驗包括哪些?甘肅個性化臨床前動物實驗是什么
化學藥臨床前動物實驗機構;西藏高質量臨床前動物實驗研究
臨床前動物實驗推薦南京英瀚斯生物。,常規流程上,疫苗研發從細胞水平的體外實驗、到臨床前動物實驗,再到人體臨床試驗,是一個漫長的過程。證明疫苗安全有效的過程非常緩慢,從少數人的臨床試驗,只是觀察免疫反應副作用等,到需要成千上萬人來測試疫苗效果的大型試驗,這一過程至少需要1年時間。與動物疫苗在實驗室獲得結果不同,評價人的疫苗有效性依賴于長時間的統計數據,我們需要在一定時間內監測注射疫苗者與注射安慰劑者的***率的差別,而在這個過程中,通常還會有各種影響因素干擾結果,這也就是疫苗進程**拉長的原因。西藏高質量臨床前動物實驗研究
- 遼寧MCO腦缺血再灌注模型造模 2025-02-07
- 西藏專業的腦缺血再灌注模型構建 2025-02-07
- 云南靠譜的腦缺血再灌注模型多少錢 2025-02-07
- 海南專業藥物安全性評價哪家好 2025-02-06
- 河北個性化藥物安全性評價 2025-02-06
- 吉林高質量藥物安全性評價哪家好 2025-02-06
- 新疆比較好的藥物安全性評價實驗 2025-02-05
- 浙江比較好的腦缺血再灌注模型實驗 2025-02-05
- 山東腦缺血再灌注模型價格 2025-02-05
- 甘肅專門做腦缺血再灌注模型 2025-01-27
- 波絡彌達養生 2025-02-07
- 江蘇下肢矯形器支架 2025-02-07
- 紹興哪里有艾德萊RNA提取試劑盒市場報價 2025-02-07
- 山東菌燕益生元 2025-02-07
- 資生堂膠原蛋白肽口服液代工廠 2025-02-07
- 浙江眼部精華哪個好用 2025-02-07
- 天津下肢矯形器支架 2025-02-07
- 高靈敏度宿主蛋白殘留檢測試劑盒 2025-02-07
- 口服美白膠原蛋白 2025-02-07
- 陜西定做矯形器下肢器材 2025-02-07